
研究主題
缺血再灌流的病態生理
缺血再灌流(I/R)損傷發生在肝臟缺血後恢復血流時,引發的組織損傷。缺血導致氧氣缺乏和代謝產物積累,恢復血流後,過量的活性氧(ROS)引發氧化損傷和炎症反應。這一過程中,內皮細胞受損,血管通透性增加,進一步導致組織水腫和功能障礙。
最近研究顯示,外泌體(exosome)和miRNA在缺血再灌流損傷中扮演重要角色。外泌體可以傳遞炎症和氧化應激信號,而miRNA則調控關鍵的基因表達,影響細胞凋亡和炎症反應。這些分子不僅提供了對病態生理機制的深入理解,也有助於發現新的治療靶點。
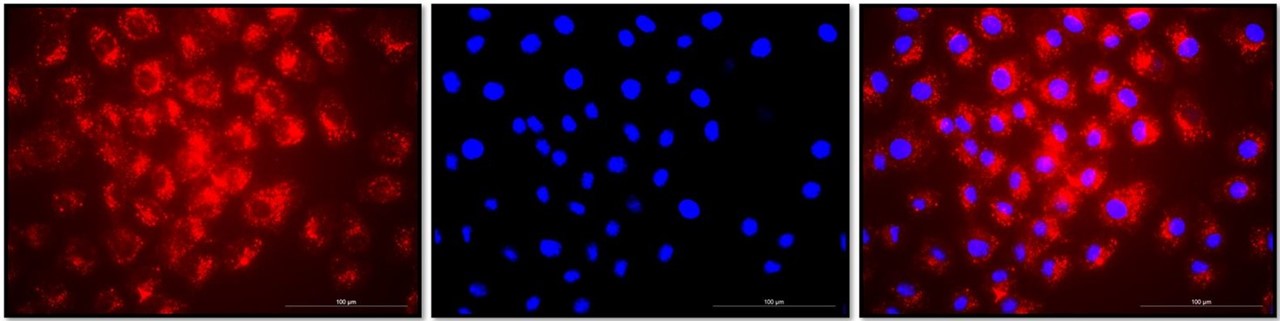
缺血再灌流
缺血再灌流是指在組織或器官經歷缺血(血流中斷)後,再次恢復血流時所引發的損傷。缺血通常導致細胞缺氧和能量耗竭,而再灌流則會引入大量氧氣,產生過量的活性氧(ROS),造成氧化損傷和細胞功能障礙。這一過程常見於肝臟移植、心臟手術或創傷後。
在缺血階段,細胞內的代謝產物積累,pH值降低,並激活應激路徑。再灌流後,氧氣重新進入受損組織,產生ROS,這些自由基會損害細胞膜、蛋白質和核酸,促使炎症反應,導致進一步的組織損傷和功能衰竭。理解這些病理過程對於改善相關臨床處置和治療策略至關重要。
外泌體和miRNA
外泌體(exosome)是直徑約30-150納米的細胞外囊泡,由細胞內多泡體(MVBs)釋放到細胞外。它們含有蛋白質、脂質、RNA(包括miRNA和mRNA)以及其他生物分子。外泌體在細胞間的通信中扮演關鍵角色,能夠將信號分子從一個細胞傳遞到另一個細胞,影響接受細胞的功能和狀態。在疾病過程中,外泌體的內容物可以反映疾病的生物標誌物,並參與調控免疫反應、腫瘤轉移及缺血再灌流損傷等過程。
miRNA是一類長度約為22個核苷酸的小RNA分子,通過靜默特定基因的表達來調節基因表達。它們通過與靶mRNA的3'非翻譯區(3' UTR)結合,抑制mRNA的翻譯或促進其降解。miRNA在多種生物學過程中發揮作用,包括細胞分化、增殖、凋亡和應激反應。在疾病如癌症、心血管病和神經退行性疾病中,miRNA的表達模式常常異常,這使得它們成為潛在的診斷和治療靶點。
外泌體和miRNA共同作用於細胞間的溝通和調控,外泌體中的miRNA能夠作為生物標誌物或治療靶點,幫助了解和治療各種疾病。
利用數位空間平台研究胃癌之腫瘤微環境及基因表達
「探索淋巴上皮樣胃癌中的細胞間交互作用與免疫微環境特徵」
淋巴上皮樣胃癌(Lymphoepithelioma-like Gastric Carcinoma, LELC)是一種罕見但獨特的胃癌類型,其腫瘤微環境中通常存在大量的免疫細胞浸潤,特別是與Epstein-Barr病毒(EBV)感染相關的案例。由於其特殊的免疫微環境,LELC對免疫治療具有潛在的敏感性。然而,腫瘤內的細胞間交互作用與基因表達特徵至今仍未被充分理解。隨著數位空間剖析技術的興起,研究者得以精確地分析腫瘤內不同區域的基因表達及其微環境特徵,進而揭示不同細胞間的相互作用。本研究旨在運用此技術深入探討LELC的腫瘤微環境及其潛在的治療靶點,以期為臨床治療策略提供新的視角與基礎。
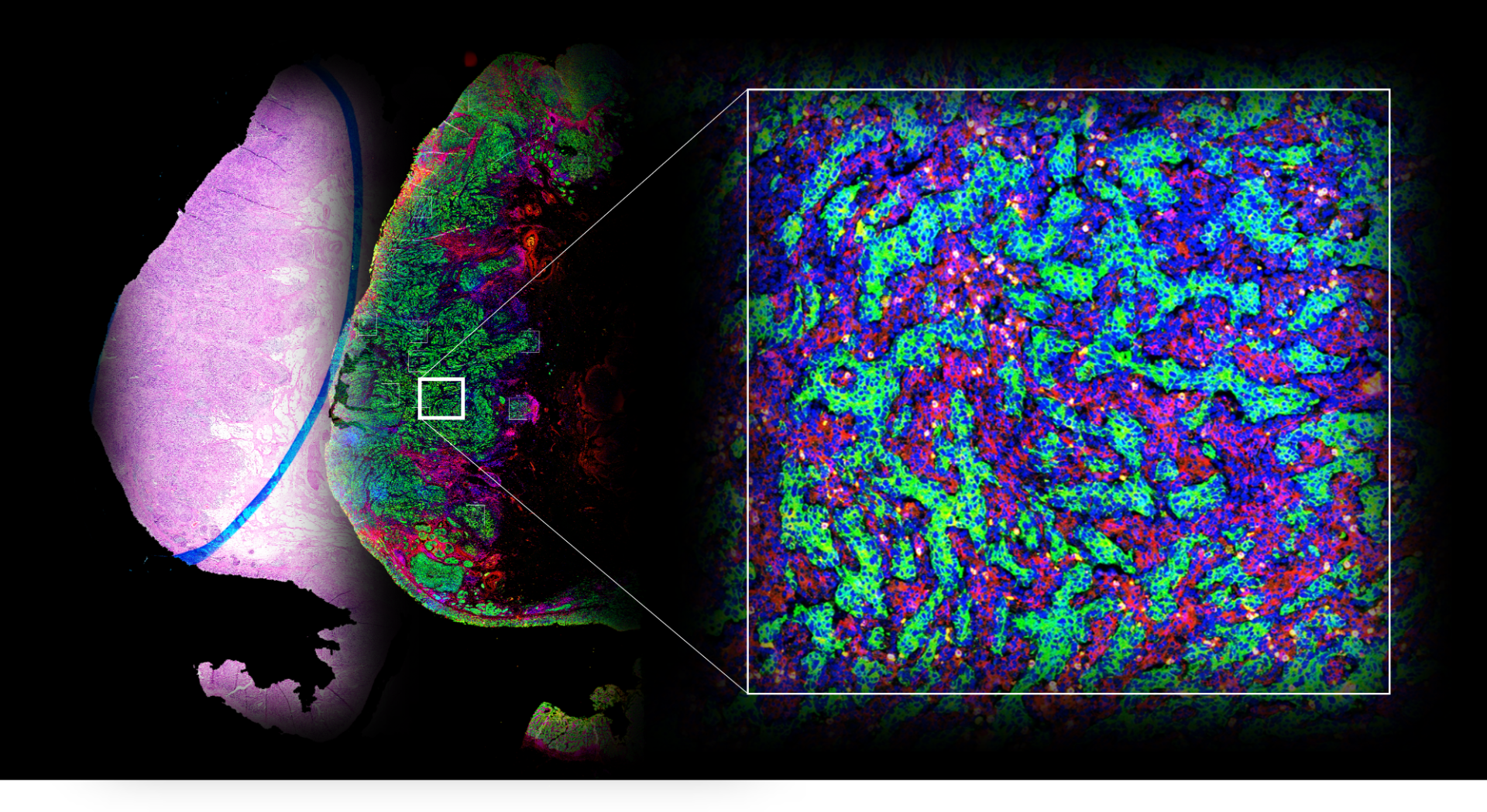
數位空間平台技術
數位空間平台 (Digital Spatial Profiling, DSP) 是一種新穎的技術,能夠在組織切片中實現精確的空間基因與蛋白質表達分析。該技術利用光學編碼和數位化定量方法,允許研究者在不破壞樣本結構的情況下,針對特定區域進行高解析度的分子檢測。透過選擇感興趣的區域或細胞群體,DSP能同時分析多個基因和蛋白質,從而提供腫瘤微環境中細胞間交互作用的深入理解。應用方面,DSP可被用來研究癌症中的異質性、免疫細胞浸潤模式,以及預測治療反應等,特別適用於探索腫瘤微環境和免疫反應的複雜結構。
淋巴上皮樣胃癌
淋巴上皮樣胃癌(Lymphoepithelioma-like Gastric Carcinoma, LELC)是一種罕見且獨特的胃癌亞型,具有高度的淋巴細胞浸潤特徵。LELC分為兩個亞型:與Epstein-Barr病毒(EBV)感染相關的亞型,以及具有高微衛星不穩定性(MSI-H)的亞型。EBV陽性亞型通常顯示出強烈的病毒誘導免疫反應,而MSI-H亞型則因DNA錯配修復缺陷而具有高突變負荷。這些亞型在腫瘤微環境中的免疫特徵各異,可能影響其對免疫療法的反應,進而影響患者的預後。因此,深入研究這兩種亞型的分子機制和免疫互動,有助於開發更具針對性的治療策略。
腫瘤微環境
腫瘤微環境(Tumor Microenvironment, TME)包括腫瘤細胞及其周圍的免疫細胞、成纖維細胞、血管內皮細胞和基質。這些組織及其分泌物共同影響腫瘤的生長、侵襲與轉移,並且不是靜態的,而是動態變化的。對於胃癌,TME在免疫療法中的角色尤為關鍵。了解TME中免疫細胞的狀態和分子特徵,能預測免疫檢查點抑制劑的療效。不同胃癌亞型,如EBV陽性和MSI-H,顯示出不同的微環境特徵,這對治療策略的選擇至關重要。因此,針對腫瘤微環境的研究有助於提升胃癌的治療效果並推動新療法的發展。
醣蛋白在胃癌轉移、生長的角色
醣蛋白是一類含有糖基化修飾的蛋白質,廣泛存在於細胞膜和細胞外基質中。在胃癌中,醣蛋白通過影響腫瘤細胞的黏附、侵襲性和轉移性,對腫瘤的生長和進展起著關鍵作用。醣蛋白的糖基化模式可以調節腫瘤細胞的信號傳導、細胞間的相互作用以及腫瘤微環境的改變。特定的醣蛋白,如MUC家族蛋白,已被證實參與胃癌的轉移過程,通過促進腫瘤細胞與基質的互動和調節免疫反應來促進腫瘤的擴散。研究醣蛋白在胃癌中的作用有助於揭示腫瘤生物學的複雜性,並可能為胃癌的診斷和治療提供新的策略。
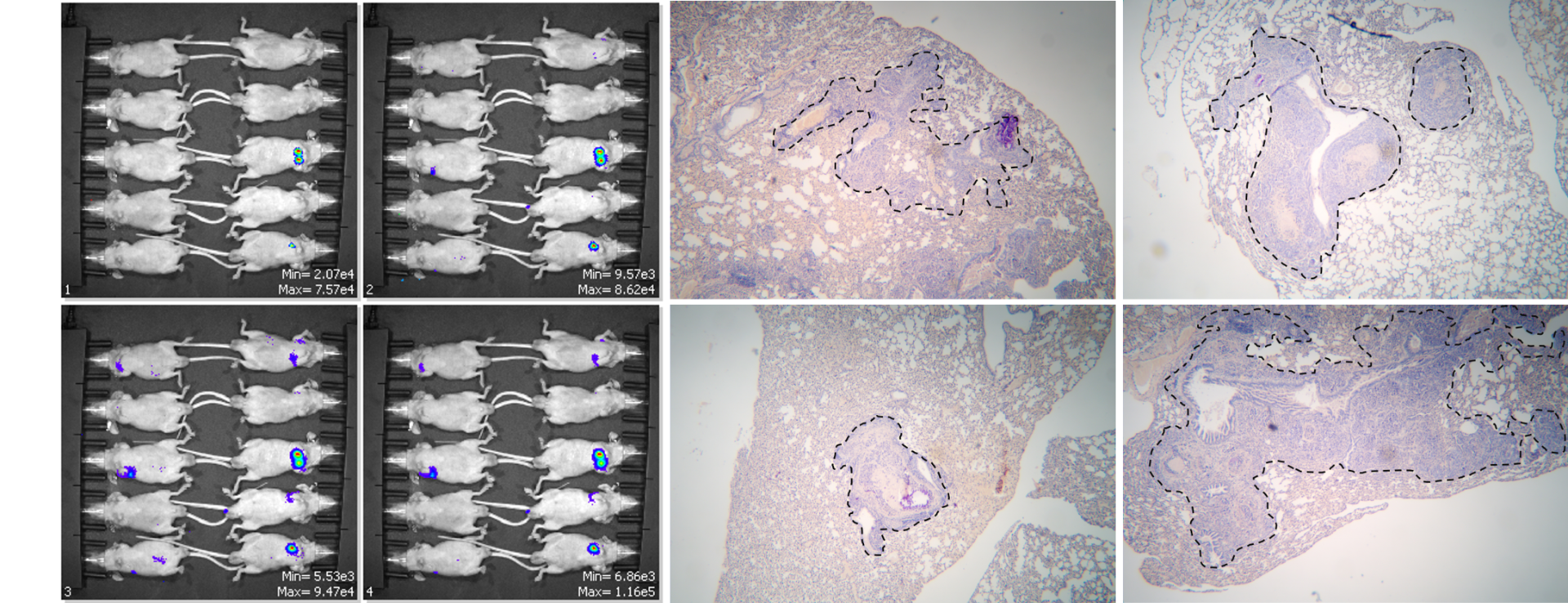
MUC20粘膜蛋白
MUC20是粘膜蛋白家族中的一員,主要在上皮細胞中表達。它具有保護和支持上皮組織的功能,通過形成保護性黏液層來防禦外界刺激。MUC20的異常表達與多種疾病,包括癌症的發展和進展有關。其在腫瘤中的作用包括改變細胞黏附性、影響細胞增殖及凋亡等。
胃癌轉移
胃癌轉移指的是胃癌細胞從原發腫瘤部位擴散到其他部位的過程。這一過程涉及腫瘤細胞的侵襲、血液或淋巴系統的轉運以及在新部位的生長。轉移性胃癌通常具有較差的預後,因為它會影響多個器官,並使治療變得更加困難。胃癌轉移的機制包括細胞間黏附的改變、基質降解和腫瘤微環境的調整。研究轉移過程中的關鍵分子和路徑對於開發新的治療策略至關重要
胃癌淋巴結轉移模式的系統發育研究
胃癌患者的淋巴轉移程度與治療策略及預後密切相關。一項隨機試驗顯示,接受廣泛淋巴切除術的晚期胃癌患者,其5年存活率優於僅接受有限切除的患者,暗示腫瘤細胞可能在擴散至遠處器官前,先行侵入第二層淋巴結(LN)。這一臨床觀察提出了區域淋巴轉移可能受到嚴格選擇而非單純被動擴散的可能性。我們利用突變率較高的多鳥嘌呤序列中的遺傳變異,來從系統發育學角度研究胃癌的淋巴轉移模式。
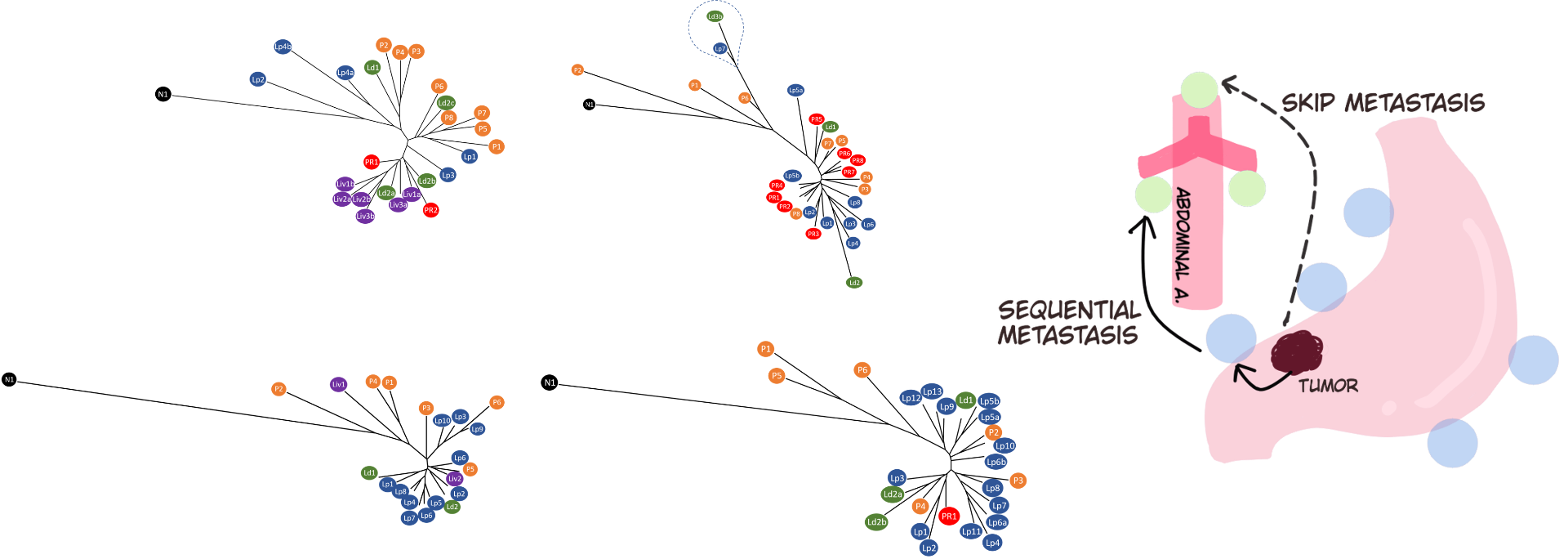
多鳥嘌呤序列
多鳥嘌呤序列(polyguanine sequences)是由連續的鳥嘌呤(guanine)核苷酸組成的DNA序列。這些序列在基因組中屬於高度突變的區域,其突變率比其他序列高出約100至10,000倍。這種高突變性使得多鳥嘌呤序列成為研究基因變異和遺傳學研究中的重要工具,尤其是在探索腫瘤進化、遺傳多樣性以及疾病機制方面。由於其突變速率高,多鳥嘌呤序列能夠提供關於基因變異模式和細胞進化過程的有價值信息。
腫瘤細胞擴散的選擇性機制:
胃癌中的第二層淋巴結轉移
在胃癌(GC)的進展過程中,腫瘤細胞在擴散到遠處器官之前,可能會先侵入第二層淋巴結(LN)。這種現象提示了胃癌腫瘤細胞的轉移過程可能比單純的被動擴散更為複雜,且涉及到一定的選擇性機制。
具體來說,第一層淋巴結(即最接近腫瘤原發部位的淋巴結)通常是腫瘤細胞初期轉移的主要目標。然而,腫瘤細胞可能會進一步擴散到第二層淋巴結,即那些位於更遠位置的淋巴結,這表明腫瘤細胞在擴散過程中並非完全被動,而是可能受到一些選擇性機制的影響。
這種腫瘤細胞的轉移模式強調了淋巴系統在腫瘤擴散中的重要角色,也提示我們在制定治療策略時應考慮到這些可能的轉移路徑。例如,這種觀察支持了進行更廣泛淋巴結切除術(如D2切除術)的必要性,因為它可能有助於提高患者的生存率並改善預後。了解腫瘤細胞如何在淋巴系統中擴散,可以幫助醫療專業人員更好地預測癌症進展,並制定更有效的治療方案。
